Набіксімолс
 | |
|---|---|
Набіксімолс
| |
| Систематизована назва за IUPAC | |
| Класифікація | |
| ATC-код | N02 |
| PubChem | |
| CAS | 56575-23-6 |
| DrugBank | |
| Торгівельне найменування |
Sativex |
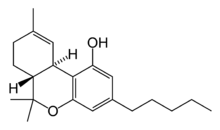
| Хімічна структура | |
| Формула | |
| Мол. маса | |
| Фармакокінетика | |
| Біодоступність | |
| Метаболізм | |
| Період напіввиведення | |
| Екскреція | |
| Реєстрація лікарського засобу в Україні | |
Набіксімолс (торгова марка «Сатівекс» (Sativex)) — пероральний спрей, розроблений британською компанією GW Pharmaceuticals для полегшення болю і спазмів, пов'язаних з розсіяним склерозом. Відрізняється від інших препаратів, що містять медичний канабіс, тим, що тетрагідроканабінол (ТГК) та канабідіол (КБД), що входять до його складу, не синтетичні ізомери (як Марінол або Набілон), а натурального походження. Доктор Вільям Ноткут, один з головних дослідників, які розробили препарат, заявив, що вивчення розсіяного склерозу як хвороби «було тісно пов'язане з політикою»[1].
Даний лікарський препарат стандартизований по композиції, формулі та дозі (для порівняння: до складу конопель входить лише приблизна кількості активних компонентів, часто відрізняються від сорту до сорту). Його основні активні компоненти — канабіноїди: ТГК і КБД. Продукт призначений для перорального прийому (спрей). У кожній дозі (одне натискання) міститься рівно 2,7 мг ТГК і 2,5 КБД.
Схвалено Міністерством охорони здоров'я Канади. Є першим в світі медикаментом, що має в складі натуральні компоненти конопель. Він також доступний у Великій Британії як неліцензований медикамент, що імпортується з Канади, щоб задовольнити потреби окремих пацієнтів і в Каталонії (Іспанія), де близько 600 осіб страждають від розсіяного склерозу.
У грудні 2005 року, GW та іспанська фармацевтична компанія Almirall оголосили ексклюзивний контракт про поширення препарату в Європі. У Великій Британії та Канаді, компанія Bayer HealthCare є ексклюзивним дистриб'ютором цього медикаменту.
На початку 2006 року препарат отримав дозвіл від FDA на початок третьої фази випробувань, але 22 березня 2007 року випробування були закриті.
У клінічних випробуваннях препарат показав себе досить толерантним.[2][3][4]
Для порівняння: дронабінол (комерційна назва — «Марінол»), синтетичний ізомер ТГК.
7 квітня 2021 р. Кабінет Міністрів України опублікував постанову № 324 «Про внесення змін до переліку наркотичних засобів, психотропних речовин і прекурсорів». З квітня 2021 року в Україні у формі лікарських засобів та за приписом лікаря дозволено використовувати, окрім Дронабінолу, ще Набілон та Набіксімолс[5].
- ↑ Greenberg, Gary (11 січня 2005). Respectable Reefer. Mother Jones. Архів оригіналу за 9 лютого 2009. Процитовано 3 квітня 2007.
- ↑ Wade D., Makela P., Robson P., House H., Bateman C. Do cannabis-based medicinal extracts have general or specific effects on symptoms in multiple sclerosis? A double-blind, randomized, placebo-controlled study on 160 patients // Mult Scler[en] : journal. — 2004. — Vol. 10, no. 4 (25 December). — P. 434—441. — PMID 15327042.
- ↑ Wade D., Makela P., House H., Bateman C., Robson P. Long-term use of a cannabis-based medicine in the treatment of spasticity and other symptoms in multiple sclerosis // Mult Scler[en] : journal. — 2006. — Vol. 12, no. 5 (25 December). — P. 639—645. — PMID 17086911.
- ↑ Wade D., Robson P., House H., Makela P., Aram J. A preliminary controlled study to determine whether whole-plant cannabis extracts can improve intractable neurogenic symptoms // Clin Rehabil[en] : journal. — 2003. — Vol. 17, no. 1 (25 December). — P. 21—9. — PMID 12617376.
- ↑ Медичний канабіс. Чи справді Україна його дозволила. https://www.bbc.com (укр.). BBC. NEWS. Україна. 12 квітня 2021. Архів оригіналу за 19 липня 2021. Процитовано 19 липня 2021.
- http://www.gwpharm.com/ [Архівовано 19 липня 2021 у Wayback Machine.] Офіційний вебсайт GW Pharmaceuticals
