Сіалові кислоти
Сіалові кислоти — клас альфа-кетокислотних вуглеводів з дев'ятьма вуглецевими атомами в ланцюгу [1]. Термін «сіалова кислота» (від грецького «слина», σίαλον — síalon) вперше був введений шведським біохіміком Гуннаром Бліксом у 1952 році. Найпоширенішим представником цієї групи є N-ацетилнейрамінова кислота, виявлена в тварин і деяких прокаріотів, яку ще називають сіаловою кислотою.

Сіалові кислоти широко поширені в тканинах тварин, а споріднені форми зустрічаються і в інших організмах, таких як деякі мікроводорості[2], бактерії та археї[3][4]. Сіалові кислоти зазвичай входять до складу глікопротеїнів, гліколіпідів або гангліозидів, де вони декорують кінці вуглецевих ланцюгів на поверхні клітин або розчинних білків. Вони також спостерігалися в ембріонах дрозофіли та деяких інших комах[5]. Рослини, як правило, не містять сіалових кислот.
У людей головний мозок має найвищий вміст сіалових кислот, де ці кислоти відіграють важливу роль у нервовій передачі та структурі гангліозидів у синаптогенезі. Відомо понад 50 видів сіалової кислоти, всі з яких можна отримати з молекули нейрамінової кислоти заміщенням її аміногрупи чи одної з її гідроксильних груп. Зазвичай аміногрупа з'єднується з ацетильною або гліколільною, але були описані й інші модифікації. Показано, що ці модифікації разом із зв’язками є тканиноспецифічними та регульованими експресіями розвитку, тому деякі з них зустрічаються лише на певних типах глікокон’югатів у конкретних клітинах. Гідроксильні групи можуть з'єднуватися з різноманітними замісникамии; так, знайдено ацетильну, лактильну, метильну, сульфатну і фосфатну групи.
Сімейство сіалових кислот включає цілий ряд похідних нейрамінової кислоти, але ці кислоти рідко зустрічаються у вільному вигляді. Зазвичай їх можна знайти як компоненти олігосахаридних ланцюгів муцинів, глікопротеїнів і гліколіпідів, які займають кінцеві, невідновлюючі позиції складних вуглеводів як на зовнішніх, так і на внутрішніх мембранах, де вони відкриті та виконують важливі функції[6].
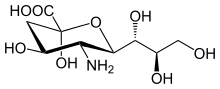
Нумерація структури сіалової кислоти починається з карбоксильного атому вуглецю. Конфігурація, в якій карбоксилат-аніон знаходиться в аксіальному положенні, є α-аномером.
Альфа-аномер - це форма, яка виникає, коли сіалова кислота зв'язується з гліканами. Однак у розчині вона переважно (понад 90%) знаходиться в бета-аномерній формі. Було виявлено бактеріальний фермент із мутаротазною активністю сіалової кислоти, NanM, який здатний швидко врівноважувати розчини сіалової кислоти до рівноважного положення спокою приблизно 90% бета/10% альфа.
На відміну від інших тварин люди генетично не здатні виробляти варіант сіалової кислоти N-гліколілнейрамінову кислоту (Neu5Gc). Виявлені в тканинах людини невеликі кількості Neu5Gc можуть бути привнесені з екзогенних (харчових) джерел[7].
Сіалова кислота синтезується глюкозамін-6-фосфатом і ацетил-КоА через трансферазу, в результаті чого утворюється N -ацетилглюкозамін-6-P. Ця сполука перетворюється на N -ацетилманнозамін-6-P шляхом епімеризації, який реагує з фосфоенолпіруватом, утворюючи N -ацетилнейрамін-9-P (сіалова кислота). Щоб вона стала активною для участі в процесі біосинтезу олігосахаридів у клітині додається монофосфатнуклеозид, який походить із цитидинтрифосфату, перетворюючи сіалову кислоту на цитидинмонофосфат-сіалову кислоту (CMP-сіалова кислота). Ця сполука синтезується в ядрі тваринної клітини[8][9].
У бактеріальних системах сіалові кислоти також можуть біосинтезуватися альдолазою. Цей фермент використовує, наприклад, похідне манози як субстрат, вставляючи три атоми вуглецю з пірувату в отриману структуру сіалової кислоти. Ці ферменти можуть бути використані для хемоферментного синтезу похідних сіалової кислоти[10].
Синтез і розпад сіалової кислоти відбуваються в різних відділах клітини. Синтез починається в цитозолі, де N -ацетилманнозамін 6 фосфат і фосфоенолпіруват утворюють сіалову кислоту. Пізніше фосфат Neu5Ac 9 активується в ядрі за допомогою залишку цитидинмонофосфату (CMP) через CMP-Neu5Ac синтазу. Хоча зв’язок між сіаловою кислотою та іншими сполуками має тенденцію бути α-зв’язуванням, цей специфічний зв’язок є єдиним, який є β-зв’язком. Потім CMP-Neu5Ac транспортується до ендоплазматичного ретикулуму або комплексу Гольджі, де він може бути перенесений до олігосахаридного ланцюга, перетворюючись на новий глікокон’югат. Цей зв'язок може бути модифікований О - ацетилюванням або О - метилюванням. Коли глікокон'югат дозріє, він транспортується на поверхню клітини.
Сіалідаза є одним з найважливіших ферментів катаболізму сіалової кислоти. Це може викликати видалення залишків сіалової кислоти з клітинної поверхні або сіалоглікокон'югатів сироватки. Зазвичай у вищих тварин глікокон'югати, які схильні до деградації, захоплюються ендоцитозом. Після злиття пізньої ендосоми з лізосомою лізосомальні сіалідази видаляють залишки сіалової кислоти. Активність цих сіалідаз заснована на видаленні O-ацетильних груп. Через мембрану лізосоми вільні молекули сіалової кислоти транспортуються в цитозоль. Там їх можна переробити та знову активувати, щоб утворити ще одну зароджувану молекулу глікокон’югату в апараті Гольджі. Сіалові кислоти також можуть розкладатися до ацилманнозаміну та пірувату за допомогою цитозольного ферменту ацилневрамінат-ліази.
Деякі важкі захворювання можуть залежати від наявності або відсутності певних ферментів, пов'язаних з метаболізмом сіалової кислоти. Сіалідоз і дефіцит сіалової кислоти з мутаціями в гені NANS можуть бути прикладами цього типу розладу[11].
З сіаловими кислотами пов'язана низка різних захворювань, що спостерігаються у людей.
Двоалельні рецесивні мутації в гені синтезу сіалової кислоти, синтази N-ацетилнейрамінової кислоти ( NANS ), у людей можуть призвести до важкого захворювання, що супроводжується інтелектуальною недостатністю та низьким зростом, що підкреслює важливість сіалової кислоти для розвитку мозку. Терапевтичні дослідження з короткочасним прийманням сіалової кислоти внутрішньо не продемонстрували помітного сприятливого впливу на біохімічні параметри
Хвороба Салла є надзвичайно рідкісним захворюванням, яке вважається найлегшою формою порушень накопичення вільної сіалової кислоти, хоча її дитяча форма вважається агресивним варіантом і люди, які страждають на неї, мають розумову відсталість. Це аутосомно-рецесивний розлад, спричинений мутацією 6-ї хромосоми. В основному впливає на нервову систему і спричинене порушенням накопичення в лізосомах, яке виникає внаслідок дефіциту специфічного носія сіалової кислоти, розташованого на мембрані лізосоми. Наразі не існує ліків від цієї хвороби та її лікування підтримувальне, зосереджене на контролі симптомів.
Усі штами вірусу грипу А потребують сіалової кислоти для зв’язування з клітинами. Існують різні форми сіалових кислот, які мають різну спорідненість із різновидом вірусу грипу А. Ця різноманітність є важливим фактом, котрий визначає, які види можуть бути заражені. Коли певний вірус грипу А розпізнається рецептором сіалової кислоти, клітина має тенденцію до ендоцитозу вірусу, що призводить до інфікування.
- ↑ Varki, Ajit; Roland Schauer (2008). Sialic Acids. in Essentials of Glycobiology. Cold Spring Harbor Press. с. Ch. 14. ISBN 9780879697709.
- ↑ Wagstaff, Ben (2018). Identification of a Kdn biosynthesis pathway in the haptophyte Prymnesium parvum suggests widespread sialic acid biosynthesis among microalgae. Journal of Biological Chemistry. 293 (42): 16277—16290. doi:10.1074/jbc.RA118.004921. PMC 6200933. PMID 30171074.
- ↑ Ajit, Varki (2017). Sialic Acids and Other Nonulosonic Acids. Sialic acids and other nonulosonic acids." Essentials of Glycobiology. Cold Spring Harbor Laboratory Press.
- ↑ Kleikamp, Hugo (2020). Tackling the chemical diversity of microbial nonulosonic acids – a universal large-scale survey approach. Chemical Science. 11 (11): 3074—3080. doi:10.1039/c9sc06406k. PMC 8157484. PMID 34122812.
- ↑ Mandal, C. (1990). Sialic acid binding lectins. Experientia. 46 (5): 433—441. doi:10.1007/BF01954221. PMID 2189746. S2CID 27075067.
- ↑ Wang, B.; Brand-Miller, J. (2003). The role and potential of sialic acid in human nutrition. European Journal of Clinical Nutrition. 57 (11): 1351—1369. doi:10.1038/sj.ejcn.1601704. PMID 14576748.
- ↑ Tangvoranuntakul, Pam (14 жовтня 2003). Human uptake and incorporation of an immunogenic nonhuman dietary sialic acid. PNAS. 100 (21): 12045—12050. Bibcode:2003PNAS..10012045T. doi:10.1073/pnas.2131556100. PMC 218710. PMID 14523234.
- ↑ Fulcher CA, "MetaCyc Chimeric Pathway: superpathway of sialic acid and CMP-sialic acid biosynthesis", "MetaCyc, March 2009"
- ↑ Warren, Leonard; Felsenfeld, Herbert (1962). The Biosynthesis of Sialic Acids (PDF). The Journal of Biological Chemistry. 237 (5): 1421. doi:10.1016/S0021-9258(19)83718-3.
- ↑ Hai Yu; Harshal Chokhawala; Shengshu Huang; Xi Chen (2006). One-pot three-enzyme chemoenzymatic approach to the synthesis of sialosides containing natural and non-natural functionalities. Nature Protocols. 1 (5): 2485—2492. doi:10.1038/nprot.2006.401.
- ↑ Traving, C.; Schauer, R. (1998). Structure, function and metabolism of sialic acids. Cellular and Molecular Life Sciences. 54 (12): 1330—1349. doi:10.1007/s000180050258. PMC 7082800. PMID 9893709.


