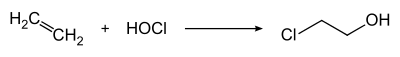Гіпохлоритна кислота
| Гіпохлоритна кислота | |
|---|---|

| |

| |
| Інші назви | Хлорноватиста кислота |
| Ідентифікатори | |
| Номер CAS | 7790-92-3 |
| Номер EINECS |
232-232-5 |
| DrugBank |
DB14135 |
| Назва MeSH |
D01.029.260.365, D01.210.465, D01.339.431.311 і D01.650.550.400 |
| ChEBI |
24757 |
| SMILES |
OCl[1] |
| InChI |
InChI=1S/ClHO/c1-2/h2H |
| Номер Гмеліна |
688 |
| Властивості | |
| Молекулярна формула | HClO |
| Молярна маса | 52,460 г/моль |
| Зовнішній вигляд | безбарвна або з жовтувато-зеленим відтінком (лише у розчині) |
| Кислотність (pKa) | 7,40 |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-120,9 кДж/моль |
| Пов'язані речовини | |
| Інші аніони | хлоридна кислота |
| Інші катіони | гіпохлорит натрію, гіпохлорит кальцію |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Гі́похлори́тна кислота́ — слабка кислота складу HClO, яка утворює ряд солей гіпохлоритів. Є дуже нестійкою сполукою і може існувати тільки в розведеному (до 30 %) розчині, в якому також продовжує розкладатися, особливо під впливом сонячного світла. Сполука проявляє сильні окисні властивості.
Застосовується для знезараження води та, рідше, як відбілювач і окисник.
Гіпохлоритну кислоту не вдалося виділити як окрему речовину через її нестійкість, вона існує лише у вигляді розчинів. Максимальна концентрація в розчині досягає 30 % (але тільки при температурах нижче -20 °C). Водні розчини є безбарвними або з жовтувато-зеленим відтінком при більших концентраціях. Може екстрагуватися в етери.
Гіпохлоритну кислоту синтезують пропусканням хлору крізь воду. В результаті хлор диспропорціонує з утворенням гіпохлоритної та хлоридної кислот:
Дана реакція є частково зворотньою. Домогтися зміщення рівноваги в бік продуктів можна додаванням до реакційної суміші оксиду ртуті(II), який зв'язує хлорид-іони:
Таким чином отримують достатньо концентровані розчини HClO. Замість оксиду HgO можна використовувати більш доступний та безпечний гідрокарбонат кальцію:
Також синтезують гіпохлоритну кислоту пропусканням суміші вологого хлору та повітря крізь колону з HgO, і подальшим розчиненням утвореного оксиду хлору Cl2O у воді при кімнатній температурі:
Гіпохлоритна кислота є вельми нестійкою сполукою і повільно розкладається; освітлення пришвидшує процес розкладання:
- (на світлі або вище 20 °C)
- (на світлі)
Утворений атомарний кисень окиснює гіпохлоритну кислоту до хлоратної:
- (на світлі)
Кислота активно розкладається при нагріванні:
Насичений розчин кислоти за відсутності світла може дегідратуватися з утворенням рідкого оксиду Cl2O, а взаємодія з хлоридною кислотою веде до утворення хлору:
- (без світла)
HClO проявляє слабкі кислотні властивості, реагує з лугами та гідроксидом амонію. Утворені солі гіпохлоритної кислоти називають гіпохлоритами:
Гіпохлоритна кислота є одним з найсильніших окисників.
Завдяки високій окисній здатності, HClO (у вигляді водних розчинів хлору) застосовується в органічному синтезі для добування хлоропохідних. Наприклад, реакцією етену з гіпохлоритною кислотою синтезують етиленхлоргідрин (2-хлороетанол), який є прекурсором для отримання оксирану:
Також із хлорогідринів, через стадію утворення нітрилів, синтезують β-гідроксикислоти:
Гіпохлоритна кислота досліджувалась як можливий засіб для догляду за ранами, і з початку 2016 року Управління з санітарного нагляду за якістю харчових продуктів та медикаментів США схвалило продукти, основним активним інгредієнтом яких є гіпохлоритна кислота, для використання при лікуванні ран та різних інфекцій у людей та тварин. Вона також схвалена FDA як консервант для сольових розчинів та має схвальний доступ до обробки свіжих продуктів харчування. У недавньому дослідженні було показано, що сольовий гігієнічний розчин, консервований чистою гіпохлоритною кислотою, значно знижує бактеріальне навантаження без зміни різноманітності видів бактерій на повіках. Після 20 хвилин лікування кількість бактерій стафілококів зменшилася на >99 %.
У 2020 році на українському ринку також з'явилися дезінфікуючі засоби на основі електрохімічно активованого розчину гіпохлоритної кислоти HOCl у вигляді активної речовини. Такі засоби мають широкий спектр дії та застосовуються у різних сферах використання. Безпечність використання таких засобів було доведено дослідженнями українських та міжнародних профільних інституцій.
2021 року гіпохлоритна кислота в концентрації до 200 PPM була внесена до Наказу МОЗ України від 28.03.2020 № 722 «Організація надання медичної допомоги хворим на коронавірусну хворобу (COVID-19)».
- ↑ HYPOCHLOROUS ACID
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5.
- Vogt H. Chlorine Oxides and Chlorine Oxygen Acids // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — P. 4—5. — DOI:
- Реми Г. Курс неорганической химии / А. В. Новоселова. — М. : ИИЛ, 1963. — Т. 1. — 922 с.
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Химический энциклопедический словарь / И. Л. Кнунянц. — М. : Сов. энциклопедия, 1983. — 792 с.
- Деркач Ф. А. Хімія. — Львів : Львівський університет, 1968. — 312 с.