Кон'югат антитіла з лікарським засобом
Кон'югат антитіла з лікарським засобом — це клас біофармацевтичних препаратів, розроблених як цільова терапія для лікування злоякісних пухлин.[1] На відміну від хіміотерапії, кон'югати антитіла з лікарським засобом направлені для цільового знищення пухлинних клітин, зберігаючи здорові клітини. Станом на 2019 рік близько 56 фармацевтичних компаній розробляли кон'югати антитіла з лікарським засобом.[2]
Кон'югат антитіла з лікарським засобом є складною молекулою, що складаються з антитіла, пов'язаного з біологічно активним цитотоксичним (протипухлинним) корисним доповненням або препаратом.[3] Кон'югати антитіла з лікарським засобом є прикладами біокон'югатів та імунокон'югатів.
Кон'югати антитіла з лікарським засобом поєднують націленість моноклональних антитіл із здатністю цитотоксичних препаратів вбивати ракові клітини. Вони можуть також розроблятися й для розрізнення здорової та хворої тканини.[4][5]
Протипухлинний препарат з'єднується з антитілом, яке специфічно спрямоване на певний пухлинний антиген (наприклад, білок, який можна виявити лише в пухлинних клітинах або на їх поверхні). Антитіла прикріплюються до антигенів на поверхні ракових клітин. Біохімічна реакція між антитілом і білком мішені (антигеном) запускає сигнал в пухлинній клітині, яка пізніше поглинає або впускає всередину антитіло разом із пов'язаним цитотоксином. Після того, як кон'югат засвоюється, цитотоксин вбиває пухлинну клітину.[6] Таке цільове застосування обмежує кількість побічних ефектів, і дає ширше терапевтичне вікно, ніж інші хіміотерапевтичні засоби.
Технології створення кон'югатів антитіла з лікарським засобом були представлені в багатьох публікаціях[7][8], зокрема й у низці наукових журналів.
Ліки, які були б спрямовані на пухлинні клітини та не діяли б на інші клітини, були задумані ще в 1900 році німецьким ученим, лауреатом Нобелівської премії Паулем Ерліхом.[2]
У 2001 році препарат компаній «Pfizer» і «Wyeth» гемтузумаб озогаміцин (торгова назва: «Майлотарг») отримав схвалення FDA на основі дослідження із сурогатною кінцевою точкою за прискореною процедурою схвалення. У червні 2010 року, після того, як були накопичені докази, на основі яких показана відсутність користі та значної токсичності препарату, FDA змусило компанію відкликати препарат з ринку.[9] У 2017 році гемтузумаб озогаміцин був знову допущений на ринок США.[10]
Брентуксимаб ведотин (торгова назва: «Адцетрис», маркетинг препарату проводиться компаніями «Seattle Genetics» і «Takeda Pharmaceutical»[11]) отримав схвалення FDA 19 серпня 2011 року для лікування рецидиву лімфогранульоматозу та рецидиву неходжкінської лімфоми та отримав умовну реєстрацію від Європейського агентства з лікарських засобів у жовтні 2012 року.
Трастузумаб емтанзин (адо-трастузумаб емтанзин або T-DM1, торгова назва «Кадцила», маркетинг проводиться «Genentech» і «Roche») схвалений у лютому 2013 року для лікування хворих з HER2-позитивним метастатичним раком молочної залози, які отримували попереднє лікування трастузумабом і хіміотерапію таксанами.[12][13]
Європейська комісія 30 червня 2017 року схвалила інотузумаб озогаміцин[14] як монотерапію для лікування дорослих із рецидивуючим або рефрактерним CD22-позитивним В-клітинним гострим лімфобластним лейкозом під торговою назвою «Безпонса®» (компаній «Pfizer»/«Wyeth»)[15], після чого 17 серпня 2017 року його схвалило FDA.[16]
Перший імунологічний кон'югат антитіла з лікарським засобом ABBV-3373 продемонстрував зниження активності хвороби у клінічному дослідженні ІІа фази хворих з ревматоїдним артритом[17], також з позитивними результатами пройшла перша фаза дослідження з іншим подібним кон'югатом антитіла з лікарським засобом ABBV-154, в якому проводилась оцінка побічних явищ та зміна активності захворювання у учасників, які отримували підшкірну ін'єкцію ABBV-154, дослідження ще триває.[18]
У липні 2018 року компанії «Daiichi Sankyo[en]» та «Glycotope GmbH» уклали угоду щодо дослідження комбінації пухлинно-асоційованого антитіла TA-MUC1 гатіпотузумабу компанії «Glycotope» та технології компанії «Daiichi Sankyo» для розробки кон'югату антитіл з лікарським засобом.[19]
У 2019 році «AstraZeneca» погодилася виплатити до 6,9 мільярдів доларів США за спільну розробку препарату DS-8201 з японською компанією «Daiichi Sankyo». Він призначений для заміни герцептину для лікування раку молочної залози. DS8201 має у своєму складі 8 корисних включень у порівнянні з 4 у більшості кон'югатів антитіла з лікарськими засобами.[2]
Загалом 11 кон'югатів антитіла з лікарським засобом отримали схвалення для клінічного застосування — усі для лікування злоякісних пухлин.
| Препарат | Виробник | Хвороба | Торгова назва |
|---|---|---|---|
| Гемтузумаб озогаміцин | Pfizer/Wyeth[en] | Гострий мієлобластний лейкоз | Майлотарг |
| Брентуксимаб ведотин | Seattle Genetics[en], «Millennium»/«Takeda Pharmaceutical» | Лімфогранульоматоз та неходжкінська лімфома | Адцетрис |
| Трастузумаб емтанзин | «Genentech», «Roche» | HER2-позитивний метастатичний рак молочної залози після лікування трастузумабом і майтанзиноїдом | Кадцила |
| Інотузумаб озогаміцин | «Pfizer»/«Wyeth[en]» | Рецидивуючий або рефрактерний CD22-позитивний В-клітинний гострий лімфобластний лейкоз | Безпонса |
| Полатузумаб ведотин | «Genentech», «Roche» | Рецидивуюча або рефрактерна дифузна великоклітинна В-клітинна лімфома[20] | Поліві |
| Енфортумаб ведотин | «Astellas»/«Seattle Genetics[en]» | Дорослі хворі з локально поширеним або метастатичним епітеліальним раком сечових шляхів, які отримували інгібітори PD-1 або PD-L1 і Pt-вмісну терапію[21] | Падсев |
| Трастузумаб дерукстекан | «AstraZeneca»/«Daiichi Sankyo[en]» | Дорослі хворі з неоперабельним або метастатичним HER2-позитивним раком молочної залози, які отримували дві або більше попередніх схем на основі анти-HER2[22] | Енгерту |
| Сацитузумаб говітекан | «Immunomedics[en]» | Дорослі хворі метастатичним потрійно негативним раком молочної залози, які отримували принаймні 2 попередні курси терапії, або хворі з рецидивом або рефрактерним раком з метастазуванням[23] | Тродельві |
| Белантамаб мафодотин | «GlaxoSmithKline» | Хворі з множинною мієломою із прогресуванням хвороби, незважаючи на попереднє лікування імуномодулюючим засобом, інгібітором протеасоми та антитілами до CD38[24] | Бленреп |
| Моксетумомаб пасудотокс | «AstraZeneca» | Рецидивний або рефрактерний волохатоклітинний лейкоз | Люмокситі |
| Лонкастуксимаб тезирин | «ADC Therapeutics» | Рецидивуюча або рефрактерна великоклітинна В-клітинна лімфома (включаючи дифузну великоклітинну В-клітинну лімфому, не зазначену інакше, як низькодиференційовану лімфому, так і високодиференційовану В-клітинну лімфому) після 2 або більше курсів системної терапії | Зінлонта |
| Тизотумаб ведотин-tftv | «Seagen Inc[en]» | Дорослі хворі з рецидивуючим або метастатичним раком шийки матки з прогресуванням хвороби під час або після хіміотерапії[25][26] | Тівідак |
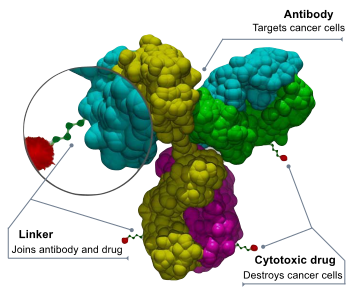
Кон'югат антитіла з лікарським засобом складається з 3 компонентів[27][28]: антитіла, яке націлено на мішень препарату, і може також спричинювати лікувальну дію. Корисне включення — спричинює бажану лікувальну дію. Лінкер — це низькомолекулярна сполука, яка приєднує корисне включення до антитіла, та має бути стабільним у кровоносному руслі, лише вивільняючи корисне включення на мішень препарату. Для приєднання до антитіла було розроблено та розглянуто кілька підходів до кон'югації.[29] Для кон'югату антитіла з лікарським засобом вираховується також співвідношення DAR, яке означає рівень співвідношення ліків і антитіл, та вказує на рівень наповненості корисним включенням кон'югату антитіла з лікарським засобом.
Багато корисних включень для онкологічних кон'югатів антитіла з лікарським засобом є природними засобами[30], що мають здатність встановлювати ковалентні зв'язки задля нейтралізації їх мішені.[31] Корисні включення включають інгібітори мікротубуліну монометил ауристатин E[32], монометил ауристатин F[33] і мертанзин[34], ДНК-зв'язуючу речовину каліхеаміцин[35] та інгібітори топоізомерази 1 SN-38[36] і ексатекан[37], що призвело до ренесансу використання природних засобів у хіміотерапії.[38] Модулятори глюкокортикоїдних рецепторів є найбільш активним класом корисних включень до кон'югатів антитіла з лікарським засобом. Були розроблені підходи до включення до складу кон'югатів давно синтезованих модуляторів глюкокортикоїдних рецепторів, зокрема дексаметазону[39][40] та будесоніду.[41] Також були розроблені модифіковані молекули модуляторів глюкокортикоїдних рецепторів[42][43], які дозволяють оптимізувати процес приєднання лінкера до корисного включення.[44] Досліджувалась також альтернатива низькомолекулярних корисних включень, зокрема малі інтерферуючі РНК.[45]
Стабільний зв'язок між антитілом і цитотоксичним (протираковим) агентом є вирішальним аспектом ефективності кон'югату антитіла з лікарським засобом.[46] Стабільний лінкер кон'югату гарантує, що буде втрачено менше цитотоксичного корисного включення, перш ніж воно досягне пухлинної клітини, покращиться безпечність препарату, та зменшиться необхідна доза препарату.
Лінкери є представниками кількох класів хімічних речовин, включаючи дисульфіди, гідразони або пептиди (розщеплювані сполуки) або тіоетери (нерозщеплювані сполуки). Під час доклінічних і клінічних досліджень було доведено, що лінкери, як ті, що розщеплюються, так і ті, що не розщеплюються, є безпечними. Брентуксимаб ведотин включає до свого складу чутливий до ферментів лінкер, що розщеплюється, який доставляє інгібітор мікротубуліну монометил ауристатин Е, що є синтетичним протипухлинним засобом, до специфічних для людини CD30-позитивних клітин злоякісних пухлин. Монометил ауристатин E пригнічує поділ клітин, блокуючи полімеризацію тубуліну. У зв'язку з високою токсичністю монометил ауристатин E не можна застосовувати як самостійний хіміотерапевтичний препарат. Однак монометил ауристатин E, пов'язаний з моноклональним антитілом проти CD30 (cAC10, білком клітинної мембрани фактора некрозу пухлини або рецептором TNF), був стабільним у позаклітинній рідині. Він розщеплюється катепсином і безпечний для застосування в лікуванні. Трастузумаб емтанзин є комбінацію інгібітора утворення мікротрубочок мертанзину та антитіла трастузумабу, яка використовує стабільний нерозщеплюваний лінкер.
Наявність кращих і стабільніших лінкерів змінила функцію хімічного зв'язку. Тип лінкера, розщеплюваний або нерозщеплюваний, надає цитотоксичному препарату специфічні властивості. Зокрема, нерозщеплюваний лінкер утримує препарат у клітині. Унаслідок цього все антитіло, лінкер і цитотоксичний (протираковий) агент потрапляють в цільову ракову клітину, де антитіло розкладається до амінокислоти. Отриманий комплекс — амінокислота, лінкер і цитотоксичний агент — вважається активним препаратом. Навпаки, лінкери, що розщеплюються, від'єднуються ферментами в раковій клітині. Цитотоксичне корисне включення може вийти з цільової клітини і в процесі, який називається «вбивство сторонніх», атакувати сусідні клітини.[47]
Інший тип розщеплюваного лінкера, який знаходиться в розробці, додає додаткову молекулу між цитотоксином і сайтом розщеплення. Це дозволяє дослідникам створювати кон'югати антитіла з лікарським засобом з більшою гнучкістю, не змінюючи кінетику розщеплення. Дослідники розробляють новий метод розщеплення пептидів, заснований на методі секвенування амінокислот у пептиді, названий розщепленням за Едманом.[48] Також розробляються сайт-специфічна кон'югація[49], та нові методи кон'югації[50][51] для подальшого покращення стабільності та терапевтичної активності кон'югату, імунокон'югати, що випромінюють α-частинки[52], наночастинки, кон'юговані з антитілами[53], та кон'югати антитіло-олігонуклеотиди.[54]
Оскільки з'явились нові форми конюгату антитіла з лікарським засобом, можливе точніше визначення точніше визначення цієї форми препарату, яке може звучати як «кон'югат чогось із лікарським засобом». Альтернативами стандартних антитіл включають декілька менших фрагментів антитіл[55], зокрема діатіла[56], Fab[57], scFV[58], та біциклічні пептиди.[59]
Перше покоління кон'югатів антитіла з лікарським засобом використовують технології зв'язування, за допомогою яких неселективно зв'язують ліки із залишками цистеїну або лізину в антитілах, внаслідок чого утворюється гетерогенна суміш. Такий підхід призводить до неоптимальної безпеки застосування препарату і його ефективності, та ускладнює оптимізацію біологічних, фізичних та фармакологічних властивостей. Сайт-специфічне включення неприродних амінокислот створює сайт для контрольованого та стабільного приєднання. Це дозволяє створювати однорідні кон'югати з антитілами, вивірено пов'язаними з препаратом, і контрольованим співвідношенням антитіла до препарату, що дозволяє вибрати найкращий у своєму класі кон'югат антитіла з лікарським засобом.[49] Відкритий безклітинний синтез на основі Escherichia coli дозволяє синтезувати білки, що містять специфічно включені неприродні амінокислоти, та оптимізований для передбачуваного високопродуктивного синтезу та згортання білка. Відсутність клітинної стінки дозволяє додавати до системи неприродні фактори, щоб керувати транскрипцією, трансляцією та згортанням білка для забезпечення точної модуляції експресії білка.[60]
Більшість кон'югатів антитіла з лікарським засобом, які розробляються або перебувають у клінічних випробуваннях, призначені для застосування при онкологічних та гематологічних захворюваннях.[61] Це в першу чергу обумовлено наявністю моноклональних антитіл, мішенню яких є різні типи раку. Однак деякі розробники прагнуть розширити застосування кон'югатів антитіла з лікарським засобом для інших груп захворювань.[62][63][64]
- ↑ Hamilton GS (вересень 2015). Antibody-drug conjugates for cancer therapy: The technological and regulatory challenges of developing drug-biologic hybrids. Biologicals. 43 (5): 318—32. doi:10.1016/j.biologicals.2015.05.006. PMID 26115630. Архів оригіналу за 11 січня 2022. Процитовано 8 травня 2022. (англ.)
- ↑ а б в Matsuyama, Kanoko (11 червня 2019). Drug to replace chemotherapy may reshape cancer care. BNN Bloomberg. Архів оригіналу за 14 червня 2019. Процитовано 14 червня 2019. (англ.)
- ↑ Fitzpatrick-Dimond, Patricia F. (9 березня 2010). Antibody-Drug Conjugates Stage a Comeback. GEN: Genetic Engineering and Biotechnology News. Архів оригіналу за 4 березня 2016. Процитовано 8 травня 2022. (англ.)
- ↑ DiJoseph JF, Armellino DC, Boghaert ER, Khandke K, Dougher MM, Sridharan L, Kunz A, Hamann PR, Gorovits B, Udata C, Moran JK, Popplewell AG, Stephens S, Frost P, Damle NK (березень 2004). Antibody-targeted chemotherapy with CMC-544: a CD22-targeted immunoconjugate of calicheamicin for the treatment of B-lymphoid malignancies. Blood. 103 (5): 1807—14. doi:10.1182/blood-2003-07-2466. PMID 14615373.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Mullard A (травень 2013). Maturing antibody-drug conjugate pipeline hits 30. Nature Reviews. Drug Discovery. 12 (5): 329—32. doi:10.1038/nrd4009. PMID 23629491. (англ.)
- ↑ Chari RV, Martell BA, Gross JL, Cook SB, Shah SA, Blättler WA, McKenzie SJ, Goldmacher VS (січень 1992). Immunoconjugates containing novel maytansinoids: promising anticancer drugs. Cancer Research. 52 (1): 127—31. PMID 1727373.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Pollack A (31 травня 2012). A One-Two Punch. The New York Times. Архів оригіналу за 8 жовтня 2021. Процитовано 8 травня 2022. (англ.)
- ↑ Ferrying a Drug Into a Cancer Cell. The New York Times. 3 червня 2012. Архів оригіналу за 3 березня 2018. Процитовано 8 травня 2022. (англ.)
- ↑ FDA: Pfizer Voluntarily Withdraws Cancer Treatment Mylotarg from U.S. Market. U.S. Food and Drug Administration. Архів оригіналу за 18 січня 2017. (англ.)
- ↑ Approved Drugs > FDA Approves Gemtuzumab Ozogamicin for CD33-positive AML. fda.gov. Silver Spring, USA: U.S. Food and Drug Administration. 1 вересня 2017. Архів оригіналу за 2 листопада 2017. Процитовано 6 вересня 2017. (англ.)
- ↑ Brentuximab vedotin (SGN35)]. ADC Review/Journal of Antibody-drug Conjugates. Архів оригіналу за 20 лютого 2015. Процитовано 8 травня 2022. (англ.)
- ↑ FDA Approves Genentech's Kadcyla® (Ado-Trastuzumab Emtansine), the First Antibody-Drug Conjugate for Treating Her2-Positive Metastatic Breast Cancer. Genentech. Архів оригіналу за 17 червня 2019. Процитовано 8 травня 2022. (англ.)
- ↑ Ado-trastuzumab emtansine. U.S. Department of Health and Human Services, National Institutes of Health, National Cancer Institute. Архів оригіналу за 25 квітня 2015. Процитовано 8 травня 2022. (англ.)
- ↑ Inotuzumab ozogamicin (drug description). ADC Review/Journal of Antibody-drug Conjugates. Архів оригіналу за 29 листопада 2020. Процитовано 8 травня 2022. (англ.)
- ↑ BESPONSA® Approved in the EU for Adult Patients with Relapsed or Refractory B-cell Precursor Acute Lymphoblastic Leukemia. 30 червня 2017. Архів оригіналу за 7 липня 2021. Процитовано 8 травня 2022. (англ.)
- ↑ U.S. FDA Approves Inotuzumab Ozogamicin for Treatment of Patients with R/R B-cell precursor Acute Lymphoblastic Leukemia. ADC Review/Journal of Antibody-drug Conjugates. 17 серпня 2017. Архів оригіналу за 17 червня 2019. Процитовано 8 травня 2022. (англ.)
- ↑ A Study to Evaluate the Safety, Tolerability, Pharmacokinetics, and Efficacy of ABBV-3373 in Participants With Moderate to Severe Rheumatoid Arthritis (RA) [Архівовано 8 травня 2022 у Wayback Machine.] (англ.)
- ↑ Study to Evaluate Adverse Events and Change in Disease Activity in Participants Between 18 to 75 Years of Age Treated With Subcutaneous (SC) Injections of ABBV-154 for Moderately to Severely Active Rheumatoid Arthritis (RA) (AIM-RA) [Архівовано 29 січня 2022 у Wayback Machine.] (англ.)
- ↑ Antibody Drug Conjugate Market Size, Share, Trends, Growth Analysis Report, Application Immunotherapy, Business Opportunity Industry, Future Trends Forecast - 2023 |. 24 вересня 2019. Архів оригіналу за 2 липня 2021. Процитовано 8 травня 2022. (англ.)
- ↑ Commissioner, Office of the (10 червня 2019). FDA approves first chemoimmunotherapy regimen for patients with relapsed or refractory diffuse large B-cell lymphoma. FDA (англ.). Архів оригіналу за 25 листопада 2019. Процитовано 14 червня 2019.
- ↑ FDA grants accelerated approval to enfortumab vedotin-ejfv for metastatic urothelial cancer. FDA (англ.). 18 грудня 2019. Архів оригіналу за 9 серпня 2020. Процитовано 3 січня 2020.
- ↑ FDA approves new treatment option for patients with HER2-positive breast cancer who have progressed on available therapies. FDA (англ.). 20 грудня 2019. Архів оригіналу за 20 грудня 2019. Процитовано 3 січня 2020.
- ↑ FDA Approves New Therapy for Triple Negative Breast Cancer That Has Spread, Not Responded to Other Treatments. FDA (англ.). 22 квітня 2020. Архів оригіналу за 23 квітня 2020. Процитовано 24 квітня 2020.
- ↑ FDA granted accelerated approval to belantamab mafodotin-blmf for multiple myeloma. FDA (англ.). 6 серпня 2020. Архів оригіналу за 6 серпня 2020. Процитовано 6 серпня 2020.
- ↑ Seagen and Genmab Announce FDA Accelerated Approval for TIVDAK™ (tisotumab vedotin-tftv) in Previously Treated Recurrent or Metastatic Cervical Cancer. Businesswire. Архів оригіналу за 11 травня 2022. Процитовано 8 травня 2022. (англ.)
- ↑ FDA Approved Antibody-Drug Conjugates (ADCs). Biochempeg. Архів оригіналу за 13 травня 2022. Процитовано 8 травня 2022. (англ.)
- ↑ Beck A, Goetsch L, Dumontet C, Corvaïa N (березень 2020). Advances in Antibody-Drug Conjugate Design: Current Clinical Landscape and Future Innovations. SLAS Discov. 25 (8): 843—868. doi:10.1177/2472555220912955. PMID 28303026. (англ.)
- ↑ Khongorzul P, Ling CJ, Khan FU, Ihsan AW, Zhang J (січень 2020). Antibody-Drug Conjugates: A Comprehensive Review. Mol Cancer Res. 18 (1): 3—19. doi:10.1158/1541-7786.MCR-19-0582. PMID 31659006. (англ.)
- ↑ Kang MS, Kong T, Khoo J, Loh TP (жовтень 2021). Recent developments in chemical conjugation strategies targeting native amino acids in proteins and their applications in antibody–drug conjugates. Chem. Sci. 12 (41): 13613—13647. doi:10.1039/D1SC02973H. PMID 34760149. (англ.)
- ↑ Gromek SM, Balunas MJ (2015). Natural products as exquisitely potent cytotoxic payloads for antibody- drug conjugates. Curr Top Med Chem. 14 (24): 2822—2834. doi:10.2174/1568026615666141208111253. PMID 30879472. (англ.)
- ↑ Vasudevan A, Argiriadi MA, Baranczak A, Friedman MM, Gavrilyuk J, Hobson AD, Hulce JJ, Osman S, Wilson NS (березень 2019). Chapter One - Covalent binders in drug discovery. Progress Med Chem. 58: 1—62. doi:10.1016/bs.pmch.2018.12.002. PMID 25487009. (англ.)
- ↑ Senter PD, Sievers EL (липень 2012). The discovery and development of brentuximab vedotin for use in relapsed Hodgkin lymphoma and systemic anaplastic large cell lymphoma. Nat Biotechnol. 30 (7): 631—637. doi:10.1038/nbt.2289. PMID 22781692. (англ.)
- ↑ Wang B, Wu C, Zhong Q, Ling L, Wu Z, Yu B, Gao X, Zeng H, Yang DH (листопад 2021). Belantamab mafodotin for the treatment of multiple myeloma. Drugs Today (Barc). 57 (11): 653—663. doi:10.1358/dot.2021.57.11.3319146. PMID 34821879. (англ.)
- ↑ von Minckwitz G, Huang CS, Mano MS, Loibl S, Mamounas EP, Untch M, Wolmark N, Rastogi P, Schneeweiss A, Redondo A, Fischer HH, Jacot W, Conlin AK, Arce-Salinas C, Wapnir IL, Jackisch C, DiGiovanna MP, Fasching PA, Crown JP, Wülfing P, Shao Z, Caremoli ER, Wu H, Lam LH, Tesarowski D, Smitt M, Douthwaite H, Singel SM, Geyer Jr CE (лютий 2019). Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer. N Engl J Med. 380 (7): 617—628. doi:10.1056/NEJMoa1814017. PMID 0516102. (англ.)
- ↑ Godwin CD, Gale RP, Walter RB (червень 2017). Gemtuzumab ozogamicin in acute myeloid leukemia. Leukemia. 31: 1855—1868. doi:10.1038/leu.2017.187. (англ.)
- ↑ Bardia A, Mayer IA, Vahdat LT, Tolaney SM, Isakoff SJ, Diamond JR, O'Shaughnessy J, Moroose RL, Santin AD, Abramson VG, Shah NC, Rugo HS, Goldenberg DM, Sweidan AM, Iannone R, Washkowitz S, Sharkey RM, Wegener WA, Kalinsky K (лютий 2019). Sacituzumab Govitecan-hziy in Refractory Metastatic Triple-Negative Breast Cancer. N Engl J Med. 380 (8): 741—751. doi:10.1056/NEJMoa1814213. PMID 30786188. (англ.)
- ↑ Ogitani Y, Aida T, Hagihara K, Yamaguchi J, Ishii C, Harada N, Soma M, Okamoto H, Oitate M, Arakawa S, Hirai T, Atsumi R, Nakada T, Hayakawa I, Abe Y, Agatsuma T (жовтень 2016). DS-8201a, A Novel HER2-Targeting ADC with a Novel DNA Topoisomerase I Inhibitor, Demonstrates a Promising Antitumor Efficacy with Differentiation from T-DM1. Clin Cancer Res. 22 (20): 5097—5108. doi:10.1158/1078-0432.CCR-15-2822. PMID 27026201. (англ.)
- ↑ Nicolaou KC, Rigol S (серпень 2019). The Role of Organic Synthesis in the Emergence and Development of Antibody-Drug Conjugates as Targeted Cancer Therapies. Angew Chem Int Ed Engl. 58 (33): 11206—11241. doi:10.1002/anie.201903498. PMID 31012193. (англ.)
- ↑ Graversen JH, Svendsen P, Dagnæs-Hansen F, Dal J, Anton G, Etzerodt A, Petersen MD, Christensen PA, Møller HJ, Moestrup SK (серпень 2012). Targeting the Hemoglobin Scavenger receptor CD163 in Macrophages Highly Increases the Anti-inflammatory Potency of Dexamethasone. Mol Ther. 20 (8): 1550—1558. doi:10.1038/mt.2012.103. PMID 22643864. (англ.)
- ↑ Svendsen P, Graversen JH, Etzerodt A, Hager H, Røge R, Grønbæk H, Christensen EI, Møller HJ, Vilstrup H, Moestrup SK (березень 2017). Antibody-Directed Glucocorticoid Targeting to CD163 in M2-type Macrophages Attenuates Fructose-Induced Liver Inflammatory Changes. Mol Ther Methods Clin Dev. 4: 50—61. doi:10.1016/j.omtm.2016.11.004. PMID 28344991. (англ.)
- ↑ Kern JC, Dooney D, Zhang R, Liang L, Brandish PE, Cheng M, Feng G, Beck A, Bresson D, Firdos J, Gately D, Knudsen N, Manibusan A, Sun Y, Garbaccio RM (вересень 2016). Novel Phosphate Modified Cathepsin B Linkers: Improving Aqueous Solubility and Enhancing Payload Scope of ADCs. Bioconjug Chem. 27 (9): 2081—2088. doi:10.1021/acs.bioconjchem.6b00337. PMID 27469406. (англ.)
- ↑ Brandish PE, Palmieri A, Antonenko S, Beaumont M, Benso L, Cancilla M, Cheng M, Fayadat-Dilman L, Feng G, Figueroa I, Firdos J, Garbaccio R, Garvin-Queen L, Gately D, Geda P, Haines C, Hseih S, Hodges D, Kern J, Knudsen N, Kwasnjuk K, Liang L, Ma H, Manibusan A, Miller PL, Moy LY, Qu Y, Shah S, Shin JS, Stivers P, Sun Y, Tomazela D, Woo HC, Zaller D, Zhang S, Zhang Y, Zielstorff M (липень 2018). Development of Anti-CD74 Antibody-Drug Conjugates to Target Glucocorticoids to Immune Cells. Bioconjug Chem. 29 (7): 2357—2369. doi:10.1021/acs.bioconjchem.8b00312. PMID 29923706. (англ.)
- ↑ Han A, Olsen O, D'Souza C, Shan J, Zhao F, Yanolatos J, Hovhannisyan Z, Haxhinasto S, Delfino F, Olson W (серпень 2021). Development of Novel Glucocorticoids for Use in Antibody-Drug Conjugates for the Treatment of Inflammatory Diseases. J Med Chem. 64 (16): 11958—11971. doi:10.1021/acs.jmedchem.1c00541. PMID 34378927. (англ.)
- ↑ Hobson AD, McPherson MJ, Waegell W, Goess CA, Stoffel RH, Li X, Zhou J, Wang Z, Yu Y, Hernandez Jr A, Bryant SH, Mathieu SL, Bischoff AK, Fitzgibbons J, Pawlikowska M, Puthenveetil S, Santora LC, Wang L, Wang L, Marvin CC, Hayes ME, Shrestha A, Sarris KA, Li B (лютий 2022). Design and Development of Glucocorticoid Receptor Modulator Agonists as Immunology Antibody-Drug Conjugate (iADC) Payloads. J Med Chem. doi:10.1021/acs.jmedchem.1c02099. (англ.)
- ↑ Yarian F, Alibakhshi A, Eyvazi S, Arezumand R, Ahangarzadeh S (August 2019). Antibody-drug therapeutic conjugates: Potential of antibody-siRNAs in cancer therapy. J Cell Physiol. 234 (10): 16724—16738. doi:10.1002/jcp.28490. PMID 30908646. (англ.)
- ↑ Beck A, Goetsch L, Dumontet C, Corvaïa N (травень 2017). Strategies and challenges for the next generation of antibody-drug conjugates. Nature Reviews. Drug Discovery. 16 (5): 315—337. doi:10.1038/nrd.2016.268. PMID 28303026. (англ.)
- ↑ Kovtun YV, Goldmacher VS (жовтень 2007). Cell killing by antibody-drug conjugates. Cancer Letters. 255 (2): 232—40. doi:10.1016/j.canlet.2007.04.010. PMID 17553616. (англ.)
- ↑ Bąchor R, Kluczyk A, Stefanowicz P, Szewczuk Z (серпень 2013). New method of peptide cleavage based on Edman degradation. Molecular Diversity. 17 (3): 605—11. doi:10.1007/s11030-013-9453-y. PMC 3713267. PMID 23690169. (англ.)
- ↑ а б Axup JY, Bajjuri KM, Ritland M, Hutchins BM, Kim CH, Kazane SA, Halder R, Forsyth JS, Santidrian AF, Stafin K, Lu Y, Tran H, Seller AJ, Biroc SL, Szydlik A, Pinkstaff JK, Tian F, Sinha SC, Felding-Habermann B, Smider VV, Schultz PG (жовтень 2012). Synthesis of site-specific antibody-drug conjugates using unnatural amino acids. Proceedings of the National Academy of Sciences of the United States of America. 109 (40): 16101—6. Bibcode:2012PNAS..10916101A. doi:10.1073/pnas.1211023109. PMC 3479532. PMID 22988081.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Lyon RP, Setter JR, Bovee TD, Doronina SO, Hunter JH, Anderson ME, Balasubramanian CL, Duniho SM, Leiske CI, Li F, Senter PD (жовтень 2014). Self-hydrolyzing maleimides improve the stability and pharmacological properties of antibody-drug conjugates. Nature Biotechnology. 32 (10): 1059—62. doi:10.1038/nbt.2968. PMID 25194818.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Kolodych S, Koniev O, Baatarkhuu Z, Bonnefoy JY, Debaene F, Cianférani S, Van Dorsselaer A, Wagner A (лютий 2015). CBTF: new amine-to-thiol coupling reagent for preparation of antibody conjugates with increased plasma stability. Bioconjugate Chemistry. 26 (2): 197—200. doi:10.1021/bc500610g. PMID 25614935.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Wulbrand C, Seidl C, Gaertner FC, Bruchertseifer F, Morgenstern A, Essler M, Senekowitsch-Schmidtke R (2013). Alpha-particle emitting 213Bi-anti-EGFR immunoconjugates eradicate tumor cells independent of oxygenation. PLOS ONE. 8 (5): e64730. Bibcode:2013PLoSO...864730W. doi:10.1371/journal.pone.0064730. PMC 3665541. PMID 23724085.
{{cite journal}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) (англ.) - ↑ Cardoso MM, Peça IN, Roque AC (2012). Antibody-conjugated nanoparticles for therapeutic applications. Current Medicinal Chemistry. 19 (19): 3103—27. doi:10.2174/092986712800784667. PMID 22612698. (англ.)
- ↑ Dovgan I, Koniev O, Kolodych S, Wagner A (жовтень 2019). Antibody-Oligonucleotide Conjugates as Therapeutic, Imaging, and Detection Agents. Bioconjugate Chemistry. 30 (10): 2483—2501. doi:10.1021/acs.bioconjchem.9b00306. PMID 31339691. (англ.)
- ↑ Deonarain MP, Yahioglu G (червень 2021). Current strategies for the discovery and bioconjugation of smaller, targetable drug conjugates tailored for solid tumor therapy. Expert Opin Drug Discov. 16 (6): 613—624. doi:10.1080/17460441.2021.1858050. PMID 33275475. (англ.)
- ↑ Li Q, Barrett A, Vijayakrishnan B, Tiberghien A, Beard R, Rickert KW, Allen KL, Christie RJ, Marelli M, Harper J, Howard P, Wu H, Dall'Acqua WF, Tsui P, Gao C, Borrok MJ (квітень 2019). Improved Inhibition of Tumor Growth by Diabody-Drug Conjugates via Half-Life Extension. Bioconjug Chem. 30 (4): 1232—1243. doi:10.1021/acs.bioconjchem.9b00170. PMID 30912649. (англ.)
- ↑ Hwang D, Rader C (травень 2020). Site-Specific Antibody-Drug Conjugates in Triple Variable Domain Fab Format. Biomolecules. 10 (5): 764. doi:10.3390/biom10050764. PMID 32422893.
{{cite journal}}: Обслуговування CS1: Сторінки із непозначеним DOI з безкоштовним доступом (посилання) (англ.) - ↑ Aubrey N, Allard-Vannier E, Martin C, Bryden F, Letast S, Colas C, Lakhrif Z, Collinet N, Dimier-Poisson I, Chourpa I, Viaud-Massuard MC, Joubert N (листопад 2018). Site-Specific Conjugation of Auristatins onto Engineered scFv Using Second Generation Maleimide to Target HER2-positive Breast Cancer in Vitro. Bioconjug Chem. 29 (11): 3516—3521. doi:10.1021/acs.bioconjchem.8b00668. PMID 30352511. (англ.)
- ↑ Hurov K, Lahdenranta J, Upadhyaya P, Haines E, Cohen H, Repash E, Kanakia D, Ma J, Kristensson J, You F, Campbell C, Witty D, Kelly M, Blakemore S, Jeffrey P, McDonnell K, Brandish P, Keen N (листопад 2021). BT7480, a novel fully synthetic Bicycle tumor-targeted immune cell agonist™ (Bicycle TICA™) induces tumor localized CD137 agonism. J Immunother Cancer. 9 (11): e002883. doi:10.1136/jitc-2021-002883. PMID 34725211. (англ.)
- ↑ Zawada JF, Yin G, Steiner AR, Yang J, Naresh A, Roy SM, Gold DS, Heinsohn HG, Murray CJ (липень 2011). Microscale to manufacturing scale-up of cell-free cytokine production--a new approach for shortening protein production development timelines. Biotechnology and Bioengineering. 108 (7): 1570—8. doi:10.1002/bit.23103. PMC 3128707. PMID 21337337.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Flygare JA, Pillow TH, Aristoff P (січень 2013). Antibody-drug conjugates for the treatment of cancer. Chemical Biology & Drug Design. 81 (1): 113—21. doi:10.1111/cbdd.12085. PMID 23253133. (англ.)
- ↑ Lehar SM, Pillow T, Xu M, Staben L, Kajihara KK, Vandlen R, DePalatis L, Raab H, Hazenbos WL, Morisaki JH, Kim J, Park S, Darwish M, Lee BC, Hernandez H, Loyet KM, Lupardus P, Fong R, Yan D, Chalouni C, Luis E, Khalfin Y, Plise E, Cheong J, Lyssikatos JP, Strandh M, Koefoed K, Andersen PS, Flygare JA, Wah Tan M, Brown EJ, Mariathasan S (листопад 2015). Novel antibody-antibiotic conjugate eliminates intracellular S. aureus. Nature. 527 (7578): 323—8. Bibcode:2015Natur.527..323L. doi:10.1038/nature16057. PMID 26536114.
{{cite journal}}: Недійсний|display-authors=6(довідка) (англ.) - ↑ Ambrx Collaborates with Merck to Design and Develop Biologic Drug Conjugates. Архів оригіналу (Press Release) за 7 січня 2013. (англ.)
- ↑ McPherson MJ, Hobson AD (2020). Pushing the Envelope: Advancement of ADCs Outside of Oncology In: Tumey L. (eds) Antibody-Drug Conjugates, Humana, New York, NY. Methods Mol Biol. Т. 2078, № 23. с. 23—36. doi:10.1007/978-1-4939-9929-3_2. PMID 31643047. (англ.)