Неопентан
| Неопентан | |
|---|---|
 Скелетна формула неопентану
|
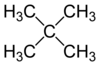 Структурна формула неопентану
|
 Кулестержнева модель молекули неопентану
| |
| Назва за IUPAC | диметилпропан |
| Ідентифікатори | |
| Номер CAS | 463-82-1 |
| Номер EINECS | 207-343-7 |
| ChEBI | 30358 |
| SMILES | CC(C)(C)C |
| InChI | InChI=1S/C5H12/c1-5(2,3)4/h1-4H3 |
| Номер Бельштейна | 1730722 |
| Номер Гмеліна | 1850 |
| Властивості | |
| Молекулярна формула | C5H12 |
| Молярна маса | 72,15 г/моль |
| Зовнішній вигляд | безбарвний газ |
| Густина | 0,627 г/см³ |
| Тпл | −16,6 °C (255 K)[1] |
| Ткип | 9,5 °C (283 K)[1] |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
−168 кДж/моль |
| Ст. ентальпія згоряння ΔcH 298 |
−3514 кДж/моль |
| Ст. ентропія S 298 |
217 Дж·K−1·моль−1 |
| Небезпеки | |
| Класифікація ЄС | |
| R-фрази | R12, R51/53 |
| S-фрази | S2, S9, S16, S33, S61 |
| NFPA 704 | |
| Температура спалаху | схильний до самозаймання |
| Пов'язані речовини | |
| Інші (алкани) | пентан ізопентан |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Неопентан — диметилпропан, C(CH3)4, ізомер нормального пентану.
Безбарвна рідина, у воді не розчиняється.
Густина d0
4 - 0,5910 г/см3; d20
4 0,613;
Температура плавлення -16,55 °C;
Температура кипіння 9,503 °C);
Критична температура 160,75 °C;
Критичний тиск 3,199 МПа;
Густина критична 237,7 кг/м3;
Температура займання 450 °C;
Показник заломлення n20
D 1,342;
Теплоємність 1,670 кДж/(кг·К) при 298,15 К;
Октанове число 85;
Довжина молекули 7,08Ǻ.
Міститься в невеликих кількостях у нафті. Може бути отримано за реакцією Вюрца взаємодією 2,2-дихлорпропану з CH3Li, (CH3)2Zn або CH3MgI. Застосовують як компонент високоякісних палив.
- ↑ а б James Wei (1999), Molecular Symmetry, Rotational Entropy, and Elevated Melting Points. Ind. Eng. Chem. Res., volume 38 issue 12, pp. 5019–5027 DOI:10.1021/ie990588m
- Петров Ал.А. Химия алканов. М.: Наука, 1974. 243 с.(рос.)
| |||||
